
高通量测序技术(NGS)以其通量大、成本低、精准度高等优势,已经在肿瘤精准医疗领域展现了广阔的应用场景。随着靶向治疗、免疫治疗、细胞治疗等多种精准疗法的临床应用,医院病理科、检验科、精准医学中心等院内实验室搭建自己的临床NGS检测平台,也开始成为一个趋势。
关于肿瘤NGS检测囊括哪些环节,最新发布的《高通量测序技术临床规范化应用北京专家共识(第一版肿瘤部分)》(以下简称“共识”)已有了详细论述。下面我们将结合共识,以吉因加肿瘤NGS一体化解决方案为例,为您揭秘一管血或一小块组织,如何经过一系列的检测方法,最后生成一份符合临床标准的检测报告。

图1 吉因加国产肿瘤NGS一体化解决方案
NGS检测步骤繁杂,但总体上可以分为湿实验和干实验两个部分1。共识指出,实验室应对检测操作全过程建立具有可操作性的SOPs2,以保证结果的可靠性和可追溯性。NGS全流程检测的每个环节及质控都对最终结果有重大影响,因此要实现共识的要求,就必须有全流程的质控体系作为支撑。在本篇中,我们以吉因加全流程质控体系为线索,为大家介绍NGS检测湿实验过程,干实验部分将在下期揭晓。
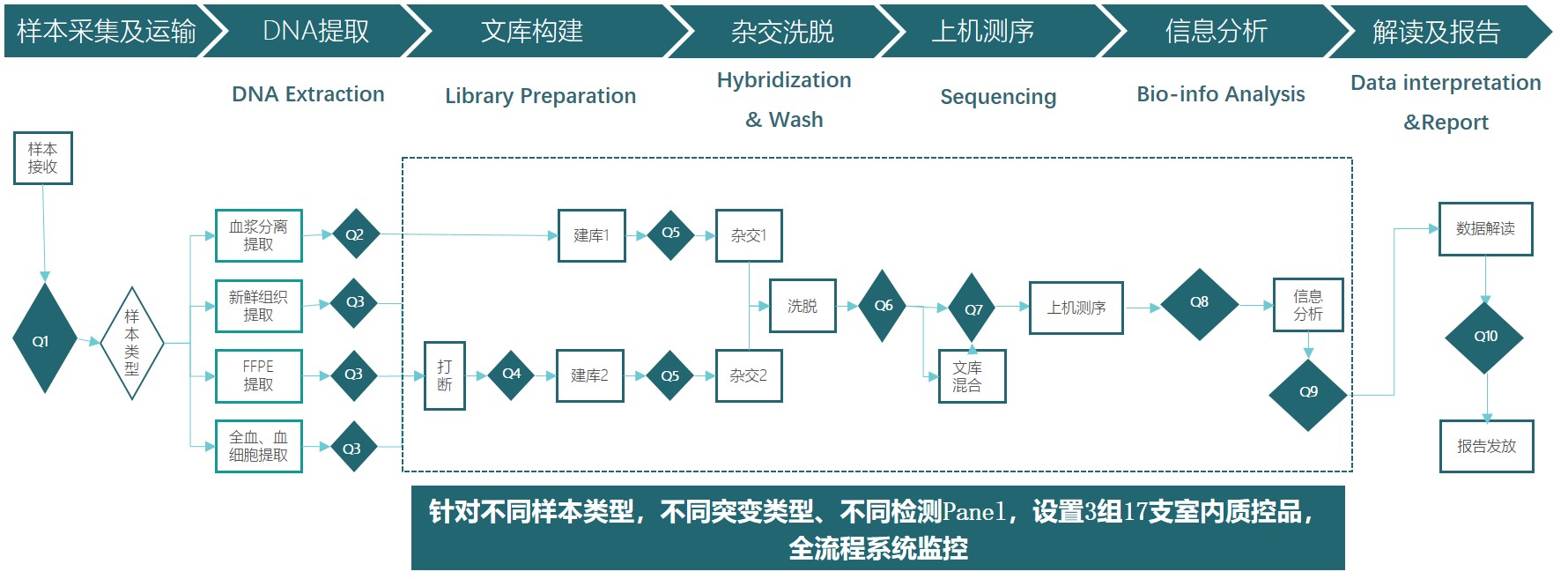
图2 全流程质控图
样本采集
肿瘤NGS检测的起点是样本收集,临床上,常见的样本类型包括:FFPE、新鲜组织、血液、胸腹水等2。而鉴于无创检测的便利性,现在越来越多的医院和实验室倾向于选择血液样本等进行检测。为保证检测质量,样本接收时首先需要根据样本运输要求和接收标准检查送检样本基础信息,如运输方式、送检单、知情同意书等,以及所采样本是否符合要求,如肿瘤细胞含量、术后采样时间、近期用药史等2(质控点①:评估送检样本是否合格)。样本合格了才可以进行检测,对于不合格的样本建议重新送检。
对确认合格后的样本要进行核酸提取,不同样本类型对核酸提取试剂的要求不同,实验室可使用商业化的试剂盒、设备或经确认的自建核酸提取方法进行核酸样本的提取。为确保检测质量,需要对提取完成的核酸样本进行质控,一般要求组织样本提取的DNA片段分布大于500bp、血浆样本提取的DNA片段集中分布于140-170bp,且质量满足二次建库为合格样本2(质控点②:评估提取的核酸样本是否合格)。
文库制备
样本处理完之后,就是文库制备环节。对于全基因组DNA样本,在文库制备之前,需将含数十亿个碱基的全基因组DNA打断成200-300bp大小的DNA片段(cfDNA无需打断),并进行样本总量和片段大小评估(质控点③:评估片段化样本是否合格)。然后在DNA片段两端加上已知序列的接头并引入特异性标签序列,这样可以方便测序仪识别每个样本的身份。
简而言之,首先进行DNA片段(cfDNA)末端修复,并加A尾;其次,进行接头连接;然后,对获得的接头连接产物进行捕获前PCR扩增(目的是放大原始DNA模板量)并引入特异性标签。对于ctDNA等液体活检样本可在PCR扩增前,使用特异性分子标签(UMIs)标记技术,以便于准确识别天然重复序列,区分低频突变和检测过程中引入的突变2。并对PCR后的文库进行质量评估(质控点④:评估中间文库是否合格)。
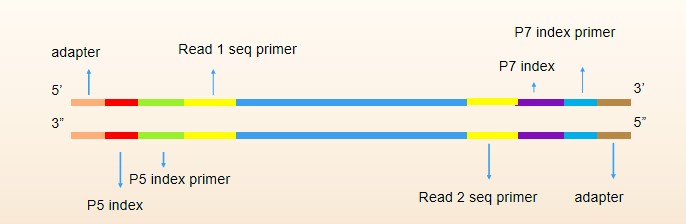
图3 文库结构示意图
对于已经构建好的中间文库样本进行靶向捕获和特异性洗脱,是为了富集目标区域。以Gene+系列基因突变检测试剂盒为例,选取特定检测目的相关的探针(生物素修饰)与中间文库进行杂交捕获,使用链霉亲和素修饰的磁珠将捕获的目标区域抓取出来,然后进行捕获之后PCR扩增,并评估样本质量和片段分布(质控点⑤:评估终文库是否合格)1,获得终文库 。
图4 Gene+人EGFR/KRAS/ALK基因突变检测试剂盒
文库制备流程的技术要求较高、操作复杂,需要消耗大量的人力和时间,可选择使用包括Gene+SP-100自动化文库制备平台在内的自动化平台进行替代。以Gene+SP-100为例,其可以完成从原始样本到产出终文库的全过程,替代至少两名高级实验员,实现85%以上文库制备过程的自动化,并且极大地缩减了实验所需空间。

图5 Gene+SP-100自动化文库制备平台
上机测序
万事俱备,湿实验的最后一步是上机测序,测序就是将这些处理好的DNA片段转化为可读取的TCGA序列。上机之前需要将终文库依次进行混合、变性及单链环化并评估环化文库质量(质控点⑥:评估环化文库总量是否合格);然后采用滚环扩增技术将单链环状DNA扩增2个数量级,生成DNA纳米球(DNA Nano Ball,DNB)(质控点⑦:评估DNB总量是否合格)。需要强调的是,与指数扩增(桥式PCR)方法不同,DNB的制备方法,始终以原始链为模板进行扩增,可以有效避免PCR的错误累积,变异检出准确度更高。
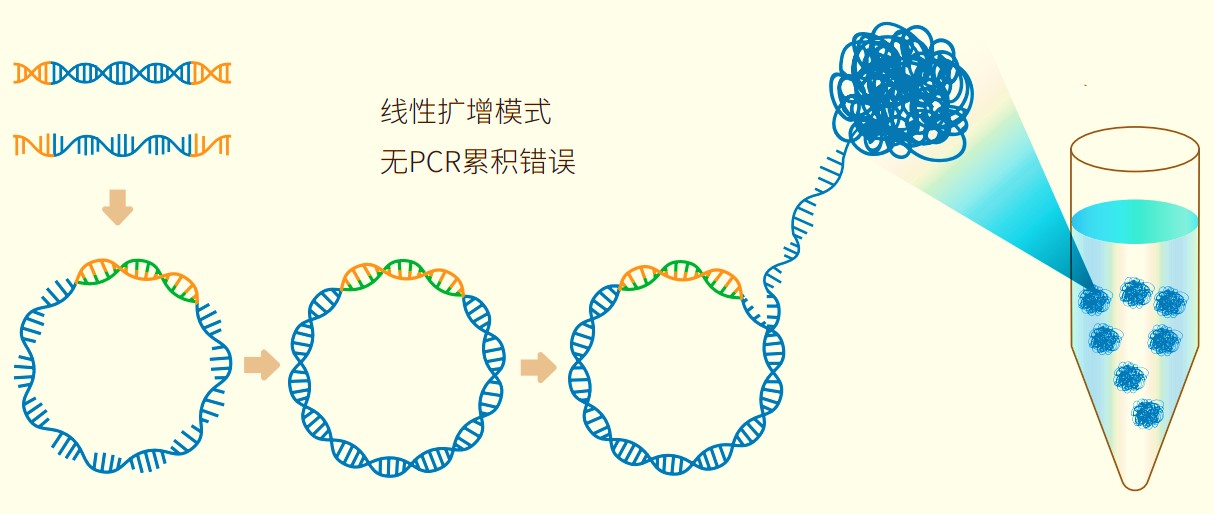
图6 DNA纳米球制备过程
最后,采用先进的联合探针锚定聚合技术和DNBSEQ技术进行测序反应,读取完整的核酸序列,以Gene+Seq-2000基因测序仪为例,数据下机之后,初级质控结果要求Q30≥85%,方可用于后续信息分析(质控点⑧:评估下机数据是否可用于后续分析)。
至此,吉因加肿瘤NGS一体化解决方案的湿实验过程就介绍完毕。后续的干实验过程中,如何实现下机数据到临床报告的自动化快速生成,我们将在下期揭晓。
参考文献:
1. 《高通量测序技术》,李金明
2.《高通量测序技术临床检测规范北京专家共识(第一版)》;王清涛,李金明,贾玫等